加入收藏 | 设为澳门新浦新京8466 | 中文 | English
 咨询热线: 028-85121781
咨询热线: 028-85121781

| Science:表观遗传可塑性与细胞间相互作用或会驱动胰腺癌的早期发生和发展 | ||||||||||||||||||||||
| [ 来源:转载自网络 发布日期:2023-06-07 10:20:58 责任编辑: 浏览次 ] | ||||||||||||||||||||||
|
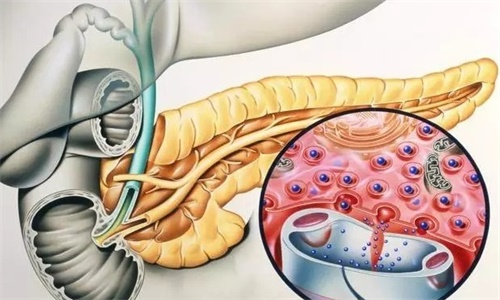
2023年5月12日,一篇发表在国际杂志Science上题为“Epigenetic plasticity cooperates with cell-cell interactions to direct pancreatic tumorigenesis”的研究报告中,来自纪念斯隆凯特琳癌症中心等机构的科学家们通过研究将复杂的遗传工程化小鼠模型与先进的计算方法相结合,成功地绘制出了导致胰腺导管腺癌(PDAC,pancreatic ductal adenocarcinoma)发生的最早期的细胞状态。
细胞摆脱其原始身份并适应环境的能力称之为可塑性(plasticity),而且这种可塑性会被炎症所增强,这些癌变前细胞能获得发送和接收远多于正常细胞的信号的能力,而且这或许并不是随机发生的,而是具有一定结构性的,当在不同的小鼠机体中进行相关实验时,研究人员就能观察到相同的模式的出现。为了研究表达突变版本的KRAS细胞的可塑性的起源和影响,研究人员利用一种遗传工程化的小鼠模型进行研究,对其正常、炎症、癌变前和恶性肿瘤组织进行单细胞分析,旨在准确重现人类胰腺癌发生的方方面面,包括从其最开始发生到最后癌症转移等。 研究人员利用基因工程小鼠模型 (GEMM)、单细胞基因组学(RNA 测序和转座酶可及染色质测序分析)和成像技术来测量胰腺上皮细胞在生理、癌前和恶性阶段的状态。这些模型促使研究人员捕捉到胰腺上皮细胞从健康状态向恶性状态进展时所发生的最早变化,这种单细胞分析也能促使研究人员有效区分每个进展阶段胰腺癌内部单一细胞亚群的特征,以及其之间的相互作用是如何驱动胰腺癌进展的。 研究人员还深入揭示了携带KRAS基因突变拷贝的细胞如何获得可塑性并在受到炎症影响时驱动癌症的进展。最后研究者表示,本文研究提供了一条路线图,其或能帮助开发新型策略,在胰腺癌进展到无法治愈的阶段前来检测甚至预防胰腺肿瘤的形成;同时,理解细胞间交流沟通网络驱动胰腺癌发生的机制也有望帮助开发新型策略,从而早期阻断或减缓癌症甚至更晚期疾病的进展。 综上,小鼠模型中肿瘤发生的多模态单细胞分析确定了胰腺癌发生的细胞和组织决定因素,可塑性的严格量化使得可塑性相关基因程序的发现成为可能,Kras突变亚群显着增加了炎症后的表观遗传可塑性,重塑了它们与免疫细胞的通讯潜力,并建立了异常的细胞间通讯回路,推动它们向肿瘤病变发展。 慎重声明:本文版权归原编辑所有,转载文章仅为传播更多信息之目的,如编辑信息标记有误,请第一时间联系大家修改或删除。
| ||||||||||||||||||||||
|
上一篇:Cancer Cell:利用癌细胞的代谢过程或有望帮助开发治疗人类胶质母细胞瘤的潜在疗法
下一篇:Cancer Cell:新型免疫疗法或能帮助机体免疫系统清除胶质母细胞瘤 |
||||||||||||||||||||||
| ||||||||||||||||||||||