�����ղ� | ��Ϊ���������¾�8466 | ���� | English
 ��ѯ���ߣ� 028-85121781
��ѯ���ߣ� 028-85121781

| ���������¾�8466ͨ������������Ƥ����άϸ����ԭ�Ĵ�л�͵�����Ԥ��UVA�յ��µ�Ƥ���ϻ� | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| [ ��Դ�����ʷ��ӿ�ѧ��־ �������ڣ�2022-08-02 16:11:30 ���α༭�� ����� ] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
�� ���ʷ��ӿ�ѧ �� ��23��13����;2022 7�� �� PMC9266774
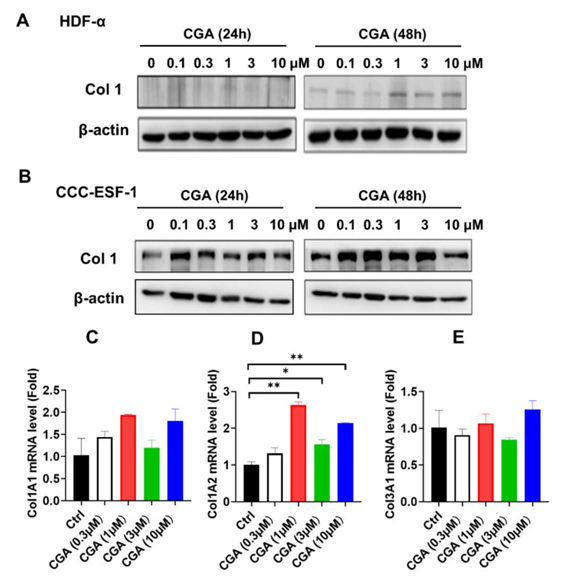
���ʷ��ӿ�ѧ��־. 2022 7��;23(13): 6941.2022 �� 6 �� 22 �����߷����� ���������¾�8466ͨ����������Ƥ����άϸ���еĽ�ԭ���״�л��ϸ����������ֹUVA�յ���Ƥ�����ϻ� Ѧ����, ��ӱ, ��, ������ ������*����ֱ�ӣ� ѧ���༭�༭��Ϣ ����ע�� ��Ȩ��������Ϣ ��؟�� �������� �� ������� �� ���ݿ��������� ת���� ���� Ƥ���ϻ���Ϊ�����ں���������Ӱ��İ�ʱ��˳���ϻ����ϻ������о�ּ��̽�ְ��������¾�8466��CGA��������Ƥ����άϸ����HDFs���Ŀ�˥������������ơ��������о��У�CGA�����Ե��ϵ���ԭ����I��Col1��mRNA�͵����ʱ�����ڲ�Ӱ��ϸ�����������������HDF����Һ�еĽ�ԭ�����ڣ�������BioMAP HDF3CGFϵͳ��Ҳ�õ���֤ʵ����������A��UVA���յ��Ĺ��ϻ��£�CGAͨ������UVA����HDF��Col1����ͽ��ͻ��ʽ�������ø1��MMP1����MMP3ˮƽ�����ڽ�ԭ���״�л��ת���������Ӧ£�TGF-�£��鵼��Smad2/3���ӵļ�����Col1�ϳ�������Ҫ�� ��UVA�������ƣ�����CGA��������ǿ�����⣬CGA������UVA�յ��Ļ�������ROS���Ļ��ۣ�������DNA���˲��ٽ�ϸ�������Ӷ�������UVA����HDF��ϸ����������֮����ҵ��о��״�֤����CGA��Ƥ�����ϻ������о��б������ã��ر�����UVA���䴥������Ϊ��һ���о�CGA����Ԥ��������Ƥ���ϻ��ṩ�����ݡ� ֤��CGA��Ƥ�����ϻ������о��б������ã��ر�����UVA���䴥������ΪCGA����Ԥ��������Ƥ���ϻ��Ľ�һ���о��ṩ�����ݡ� ֤��CGA��Ƥ�����ϻ������о��б������ã��ر�����UVA���䴥������ΪCGA����Ԥ��������Ƥ���ϻ��Ľ�һ���о��ṩ�����ݡ� �ؼ��֣� ��ԭ���ס����ʽ�������ø������Ƥ����άϸ�������ϻ������������¾�8466��UVA ����ת���� 1. �ſ� ˥����һ�������������Ĺ��̣���������Ͷ��ﲻͬ���ٺ�ϵͳ����̬��������[1].Ƥ���ϻ�ֻ����һ���̵�һ���ɼ����֣��������������ڣ����磬ʱ��˳�ɶ��ɺ��Ŵ��������ڻ���ѹ��������������ơ��ɳں�ɫ�ز�����ij��֡���Щ��֯ѧ�仯ͨ������Ƥ�н����γ�ϸ���ͺ�ɫ��ϸ��������ֳ�ͽ�ԭ��ά�����й�[2,3]. Ƥ�������Ƥ�����Ƥ�ڲ���ɣ�����ͨ������Ĥ���ӡ�I�ͽ�ԭ���ף�Col1������ḻ����Ƥϸ������ʣ�ECM���ɷ֣��뽺ԭ����III��Col3����ϣ��ڳ���Ƥ������Ƥ���γɹ㷺��ϸ������ά��Col1ռ85-90%����Col3���������Ƥ����ռ8-11%��������������Ƥ���и���Ҫ�ijɷ�[4].Col1 ��ʱ���ϻ������ͣ������ɹ��ϻ����� [5].���⣬Col1 ����ͨ��ˮ�⵰���ʣ�������ʽ�������ø ��MMP���������⣬��Щ�������ǽ��� ECM �����ձ���ڵ�����ø���� [6].��ǰ���о�������MMP-1��MMP-2��MMP-3��Ҫ�ǽ��⽺ԭ���͵��Ե���MMP[7].����Ƥ�����ϻ����̣���ԭ��������ϳɼ��٣���ԭ�����������ӣ������߶������ڽ�ԭ���������������[8,9,10].��ˣ������������ຬ�н�ԭ����Ӫ�����������ɫʳƷ�Ѿ����У��Դٽ�Ƥ���Ŀ�˥�ϡ� ��Ȼ�������ӳ�������һֱ���ڸ���Ƥ����ۣ������ܹ��գ�ɭ��ï����ȡ��ɶ��ᣬ��-�ǻ��ᣬ���ᣬ��ʾ���ȡ���������[11].������Щ��ȻС���ӻ���ȡ����ֳ����������ԣ�����ά������ƽ��ͷ�ֹ���������ߣ�UV�������Ƥ����������Ĺ��ϻ����淢�����á���Ȼ�������Ϊһ����ƣ�������������Ȼ�����еĻ�ϳɷ֣�����ʶ�����ȷ�ķ��ӽ��ʡ����������¾�8466 ��CGA�� �� L-������Ϳ������������һ����Ȼ���������������ʳ���ɲ�ҩ��ˮ�����߲��Ƴɵ������� [12].���ѱ�֤�����ж����������ԣ��������ס������������ߵ��ڡ������Ϳ���������[13,14,15,16].��һЩ�о�������CGA�Ŀ�˥�����á����磬Li�ȱ���CGA����ͨ�������Ұ���ø����������B16��ɫ����ϸ���еĺ�ɫ�����ɣ���ʾCGA��Ƥ��ɫ�س��ŵ�����[17].Cha��Her���˱�����CGA���Է�ֹUVB���������Ƥ���ϻ�[18,19,20].��Щ������CGA�Խ����γ�ϸ��������������Ƥ����ëС��ij���άϸ����UVB�յ��Ĺ��ϻ��ı��������йأ���Ϊ����Ƥ���ϻ���Ҫ��̫�������ߣ�UV�����䱩¶�й�[21].Ȼ����UVB��Ҫ���±�Ƥ������ˡ������д�Լ90-99%�ij��������ߣ�UVA�����������������Ƥ����Ƥ��֯�У����UVA��Ƥ�����ϻ�����Ҫ����[22]. ���ⷽ�棬��û���о���ʾCGA�Ƿ��Լ������������UVA�յ��Ĺ��ϻ������±�������Ƥ����άϸ�����壨HDF-����ϸ�������о��ص��о���CGA��HDFs�Ŀ����ϻ����ã��ر�����UVA����в���������Լ��뽺ԭ���״�л��ϸ��������صĻ��ơ� ת���� 2. ��� 2.1. CGA����Ƥ������άϸ����ԭ���ױ����Ӱ�� ����ͨ��������ӡ���Ͷ���RT-PCR��qRT-PCR���ⶨCGA����Ƥ������άϸ���н�ԭ���ױ����Ӱ�졣�� ͼ1��0.1��3��M�Ľϵ�Ũ����ʹ�õ�A��B��CGA������HDF-����CCC-ESF-1ϸ���е�1�ͽ�ԭ���ף�Col1�����ױ��CGA��¶48 h��Col1���ױ���Ĵ̼����ø�Ϊ���ԡ�Ϊ�˼��CGA�Խ�ԭ���Ĵ̼������Ƿ�����ת¼ˮƽ�ϣ������Col1��Col1A1��Col1A2����Col3��Col3A1��mRNA����Ļ����� ͼ1Ũ��Ϊ0.3��10��M��C-E��CGA��ǿ��Col1A1��Col1A2 mRNAˮƽ���ر�����Col1A2 mRNA�����С�CGA��1��3��10��M���Ĵ�������������Col1A2 mRNAˮƽ��Ȼ������¶CGA��Col3A1 mRNAˮƽ����û�б仯����Щ���ݱ���CGA�������յ�Col1����;��һ���������Col1A2����ת¼�Ĵٽ��� CGA����Ƥ������άϸ���н�ԭ���ױ����Ӱ�졣��HDF-��ϸ���б�¶CGA24��48Сʱ��ͨ��������ӡ���ⶨ����⽺ԭ����Iˮƽ��һ���� �� CCC-ESF-1 ϸ�� ��B).Col1A1 ��C���� Col1A2 ��D�� �� Col3A1 ��E����HDF-��ϸ������CGA����48Сʱ��ͨ��qRT-PCR�ⶨ������mRNAˮƽ����Щֵ��ʾΪ����ʵ���ƽ��ֵ��SD��* p �� 0.05�� ** p ��0.01��ʾ���������� 2.2. CGA��HDF�н�ԭ�����ڵ�Ӱ�� ��ҽ�����רע��HDF-��ϸ�������䱩¶��ָ��������CGA48Сʱ����ͨ��Biocolor Sircol����ϸ����������Һ���ܽ�ԭ���ķ������ⶨ����¶��CGA���½�ԭ�����ڵ������յ���ͼ2ͬʱ��ͨ��MTT�ⶨ�����CGA��ϸ��������Ӱ�졣 ͼ2B��ʾ��0.3��50��M֮���CGA�����ڴ���24��48��72Сʱ����Ӱ��HDF-��ϸ������ֳ���������CGA�ٽ��˽�ԭ���IJ���������Ӱ��HDF-��ϸ������ֳ�����⣬��BioMAP HDF3CGFϵͳ�У�ԭ��������������Ƥ����άϸ����HDF-n���ڴ̼�ǰ24Сʱ�����ڵ�Ѫ�������£�ϸ��������������λ�� ��1 ����ָ��������CGA�ٴ���72Сʱ����������ʮ�� ��16�� ������ ��1 ������CGA��HDF��Ӱ�졣����Щ�����У���֯���ܷ��ӽ�ԭ����I����֢���Ӹ������յ���Tϸ������ѧ���ռ���I-TAC��Ҳ��ΪCXCL11���ڸ�ϵͳ����CGA���ƺ�仯�����ԣ�ͼ3A��. Ũ��Ϊ10��50��M��CGAʹ��ԭ����I����������Լ17%��ͼ3B). CGA��HDF-��ϸ����ԭ�����ڵ�Ӱ�졣(һ������CGA��¶48Сʱ�����HDF-��ϸ������Һ�еĿ������ܽ�ԭ��������B��ͨ��MTT�ⶨ�����CGA����24��48��72Сʱ��HDF-��ϸ����ϸ���������ơ���Щֵ��ʾΪ����ʵ���ƽ��ֵ��SD��** p �� 0.01�� *** p �� 0.001 ��ʾ�����������졣 CGA��HDF�н�ԭ����I������Ӱ�졣һ��BioMAP HDF3CGFϵͳ��������CGA�Բ�����֯���ܺ���֢��16�������־������ʣ���Ӱ�졣(B����CGA������ԭ����I��������Ӱٷֱȱ���������ʾ��ֱ��ͼ�С� ��1 ɸѡ�о���ʹ�õ�BioMAP HDF3CGFϵͳ����ʾ��ϸ��������CGA�������û������������ʹ̼�72Сʱ���������г��������־�������
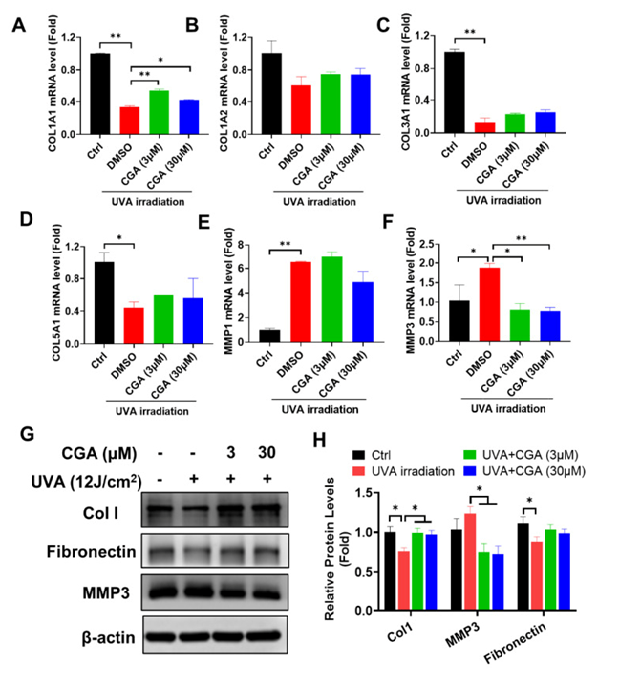
�ڵ����Ĵ����д� 2.3. CGA �� UVA ���� HDF �н�ԭ���״�л��Ӱ�� Ƥ�����ϻ�ͨ���������������йء����ڴ�ҶԷ�в��������HDFs���о�����ҽ�һ���о���CGA��UVA����������Ƥ�����ϻ������á��ر��ǣ���Ҳ����˽�ԭ����ת¼�ϳɺͽ����л�����ȣ���Ҽ����UVA�����HDF-��ϸ���в��벻ͬ��ԭ���ϳ���Ⱥ�Ĺؼ������mRNAˮƽ�� ͼ4A-D��ʾ��UVA�����I�ͽ�ԭ���ף�Col1A1����III�ͽ�ԭ���ף�Col3A1����V�ͽ�ԭ���ף�Col5A1������ˮƽ�������µ�����CGA��3��30��M�������£�UVA�����HDF-��ϸ���е�Col 1A1��������������ӣ�p �� 0.01; p ��0.05������CGA��Col3A1��Col5A1 mRNAˮƽ��Ӱ���С����һ��о���CGA��MMP�����Ӱ�죬��MMP1��MMP3��MMP9�����Dz��뽺ԭ���ķֽ⡣�뽺ԭ�����෴��UVA��������������MMP1��MMP3��mRNA���p �� 0.01; p �� 0.05; ͼ4E��F����Ȼ�����뵥����UVA������ȣ�CGA��UVA������������Ƶ���HDF-��ϸ����MMP1��MMP3ת¼���オ�͡���UVA�����HDF-��ϸ���У�MMP3 mRNAˮƽ���Ž�����3��30 ��M CGA��p �� 0.01; p ��0.01���� CGA��UVA�����HDF-��ϸ���н�ԭ����I��л��Ӱ�졣Col1A1��һ������ Col1A2 ��B���� Col3A1 ��C���� Col5A1 ��D����MMP1 ��E�� �� MMP3 ��F����UVA�����HDF-��ϸ����ͨ��qRT-PCR��⡣���ݱ�ʾ��������������ƽ����SD��* p �� 0.05�� ** p ��0.01��ʾ����������(G�� ͨ��������ӡ�����ⶨUVA�����HDF-��ϸ���е�Col1��MMP3���������ױ��(H��ͨ���ܶȲⶨ��������Ե����ʱ������ֱ��ͼ����ʾ�����������������ʵ���ƽ��ֵ��* p ��0.05��ʾ���������� ���⣬��һ�������CGA��Col1��MMP3��ͼ4G��H������mRNA����һ�£�UVA�������Ž�����Col1���ף���HDF-��ϸ���е�CGA������������ּ��١����֮�£�MMP3������������������������ӣ�����CGA��Ϻ��µ�����һ��ECM������������ˮƽ��UVA��������HDF-��ϸ���д���CGA���������ʾ����Col1���Ƶ����ơ� 2.4. CGA �� UVA ���� HDF �� TGF-��/Smad �źŴ�����Ӱ�� ̽��CGA�յ���UVA����HDF�н�ԭ�������ɵ�DZ�ڻ��ƣ�Smad2 / 3��ERK1 / 2���ӵĻ�����ǽ�ԭ���ϳɵ������ؼ��ź�ͨ·[23,24]��ͨ��������ӡ�������з�������¶��UVA�����HDF-��ϸ���е�Smad2/3���ữˮƽ���͡����UVA�����HDF-��ϸ����ȣ�UVA�����CGA���ϴ������������ữ��Smad2 / 3���Ȼ������¶��UVA����CGA��Ϻ����ữERK1 / 2��ˮƽ���ֲ��䣨ͼ5��B����
CGA��UVA����HDF-��ϸ����Smad2/3��ERK1/2�ź�ͨ·��Ӱ�졣(һ���� ͨ��������ӡ�����ⶨUVA�����HDF-��ϸ���е�p-Smad2/3��Smad2/3��p-ERK1/2��ERK1/2���ױ��(B��ͨ���ܶȲⶨ��������Ե����ʱ������ֱ��ͼ����ʾ�����ݱ�ʾΪ����ʵ���ƽ��ֵ��* p ��0.05��ʾ���������� 2.5. CGA �ɷ�ֹ UVA �յ��� HDF ϸ������ �����������������ϸ��ɱ�ˡ���ʽϸ����������ʾ����δ�����HDF-��ϸ����p �� 0.05; p �� 0.05�� ��ͼ6��B������CGA��3��30��M���������Ž�����������ϸ���ı��������磬HDF-��ϸ��������ϸ������ϸ���İٷֱȴ�UVA�������18.4%���͵�30��MCGA�������1.8%��p ��0.05������ˣ���UVA������ѽ�-PARP�ı��ϸ�������Ĺؼ�ָ�꣩�������ӣ�HDF-��ϸ����CGA�����Լ��������Է�ʽ���ͣ�ͼ6E��F���� CGA��UVA����HDF-��ϸ��ϸ��������ROS������Ӱ�졣��UVA����HDF-��ϸ��60���ӣ�Ȼ����CGA����24Сʱ���ջ�����ϸ��������ROS������(һ����ϸ�������İٷֱ�ͨ��Ĥ������V-FTC/PI˫Ⱦɫ�ⶨ���ⶨ��Ȼ�������ʽϸ�����ⶨ��(B���Ը����������еĻ�ϸ�������ں����ڵ���ϸ���Լ�����ϸ������ͳ�Ʒ��������ݱ�ʾΪ����ʵ���ƽ��ֵ��(C��ʹ��DCFH-DA̽��ͨ����ʽϸ�����ⶨ����ROS�IJ�����(DROSƽ��ӫ��ǿ�ȣ�MFI���Ǵ�����ʵ���м�������ģ�����ֱ��ͼ����ʾ��* p �� 0.05�� ** p ��0.01��ʾ����������(E�� �ѽ�� PARP �ĵ����ʱ����-H2UVA����HDF-��ϸ���е�AX��Rad51��ʹ�������Կ���ͨ��������ӡ���ⶨ���ⶨ�ġ�(F��ͨ���ܶȲⶨ��������Ե����ʱ������ֱ��ͼ����ʾ�����ݱ�ʾΪ����ʵ���ƽ��ֵ��* p �� 0.05�� *** p �� 0.001 ��ʾ�����������졣 2.6. CGA ���� UVA �յ��� ROS �� HDF �в��� Ϊ�˽�һ���˽�CGA������������������յ�ϸ����������Ҳ�����ROS�IJ������� ͼ6���������ȣ�C��D��UVA����60 min����ROSˮƽ�������ߣ�p <0.01����Ȼ����CGA��30��M�����ϴ������Ž�����UVA�����HDF-��ϸ����ϸ��ROS�Ļ��ۣ�p <0.05������-H ��ˮƽ2AX��˫�����ѣ�DSB�������еı�־���UVA�����Ҳ�������ӣ�ͼ6Ȼ����CGA��UVA�����������������˦�-H��2HDF-��ϸ���е�AX�������DNA������������־��Rad51����UVA��¶���ϵ�������CGA�������һ�����ӣ�ͼ6E). ת���� 3. ���� ��ҵ��о��״α�����CGA����ͨ���ϵ�Col1 mRNA�͵�����ˮƽ��������HDF�еĽ�ԭ��������ϳɺͷ��ڣ��ر�����1�ͽ�ԭ�����С�MMP1��MMP3��HDF-��ϸ����mRNAˮƽ��MMP9�߱����������CGA��Ӱ������HDF-��ϸ����MMP1��MMP3 mRNA�������ͼ S1A��B).��Щ���ݱ�����CGA��Ҫ�ٽ�Col1����ϳɣ��������������ڷ�в��HDF�еĽ��⡣ �����е������߷��䱻��Ϊ�ǵ���Ƥ�������ϻ�����ͻ�����������ء�����UVA���䵼�¹����ԣ����ϻ��Ͷ���Ƥ�������ķ�չ[25].����Ҫ���ǣ���֮ǰ�ı���һ��[26]����ҷ���UVA����ͨ���µ�Col1��Col3��Col5����ˮƽ���Ž��ͽ�ԭ���IJ�������ͨ���ϵ�MMP1��MMP3 mRNAˮƽ�̼���ԭ�����⡣��CGA����ʹ��������ת��UVA�����HDF-��ϸ����Col1��MMP3�ı���Ӷ�ͨ����ǿCol1�IJ����������併��������Ƥ�����ϻ�������������Ƥ������һ����Ҫ�ɷ֣���������Ƥ - ��Ƥ���紦��ɢ������CGA�����˱�¶��UVA���������ļ��٣�����CGA�ٽ�������ECM����ĺϳɡ� �������ά���������Ӻ�ϸ��������TGF-�¡�IL-4��IL-13���������άϸ����ϸ��Ĥ�����ϲ��鵼Col1����ϳɡ�TGF-�������е���Ҫ����������յ�Smad 2/3��Smad 4�γ�������帴���Ȼ������������������λ��ϸ�������Լ���ԭ��ԭ������[27].UVA������Լ���TGF-�� I��TGF-�� II����ĺϳɣ��Ӷ�����TGF-��/smad;��[23].����Ԥ�ڵ�������UVA����������HDF��Smad 2/3�źŷ��ӵĻ�� CGA����������UVA����HDF�����ữ��Smad 2/3��� ���⣬��ʹERK;����һ����Ҫ��MAPK�ź�ͨ·���佨����Ϊ�˲���Col1ת¼�ļ���[24]����ҵ��о�������p-ERK1/2�ڵ���UVA�������HDF�е�CGA����м���û�б仯����Щ���������CGAͨ���̼�UVA����HDF�е�TGF-��-Smad2/3�ź�ͨ·���ٽ�Col1��� �Ѿ�ȷ���������߷���ͨ����Ƥ����Ƥ�в����Ļ�������ROS���������ŵ�����Ӧ����ROS�Ļ���������MMP���ԣ�����ϸ������ʣ�ECM��ͨ����ԭ�����ƻ�[28]����Ҳ����DNA���˺�ϸ����������ˣ���ױƷ�е���Ȼֲ�ﻯѧ���ʣ������ǿ������������Ȳ����ӣ��Է�ֹ̫������������Ķ�����Ƥ�����������ˡ����磬�����ض�UVB��UVA�յ���ROS���������������ã���ͨ���ϵ�HDF�е�BCL2��������ֹUVA�鵼��ϸ������[29,30].�ڴ�ҵ��о��У�CGA���Ž����˦�-H2AXˮƽ��һ���ٽ���UVA����HDFs��Rad51�ı������CGA������DNA DSBs���˺������ܵĸ�����ϸ��ROS�����ļ���ͬʱ����������UVA����HDFs��ϸ�������ͻ���ϸ�������ơ� ��ȻCGA����UVA����HDF-��ϸ��������������һ�����ƺ��������й�ʵ����1���о���֤���Ŀ����Ʒ������ñ������ۣ�http://www.chinadrugtrials.org.cn ��2022 �� 1 �� 31 �շ��ʣ������ CTR20160113���Լ������ٴ������ʶ�� http://clinicaltrials.gov ����2022��1��31�շ��ʣ��� NCT02728349����һ�µ���CGA��������ֱ�ӵ�ϸ�������յ�����Ҳ��������HDF-��ϸ���е���ֳ���籾�о���ʾ��UVA������ܻᴥ��HDF-��ϸ������������ϸ����ͬ���ź�ͨ·��ͨ���������߷�Ӧ�����罺��ĸϸ�����е�M2������ΪM1������������������[15].��Ȥ���ǣ��ڹ��ϻ��ı����£���������1�������еĽ���ĸϸ�������ߣ���ҹ۲쵽һЩ���ߵ�Ƥ�����������������Ҫ���沿Ƥ����CGA����GBM����Ѫ����Col1�����ķ�����ʾ��CGA���ƺ�Col1���������ߣ�����ͼS2������������ HDF ģ���з��ֵ� Col1 ���ӵ� CGA һ����Ŀǰ�в������CGA���ƵĽ���ĸϸ����������Col1������������ֱ�ӵĻ����������á�Ȼ����Col1����������Ѫ�����ɺ���������չ��Ӱ����Ҫ�ڽ�һ�����о��в����� ����������CGA�ٽ�����δ����HDFs��Col1�ĺϳɡ����⣬CGAͨ�����ƽ�ԭ���������ǿ��ԭ���ϳ�������HDF-��ϸ������UVA�յ��Ĺ��ϻ������⣬CGA������UVA�յ���ROS�Ļ��ۣ�������DNA���˲��ٽ���ϸ������CGA��UVA�յ��Ĺ��ϻ����йⱣ����DZ�ڻ�����ʾ�� ͼ7.������������Щ����֧�Ž�һ���о�CGA��Ԥ��������Ƥ�����ϻ���ʱ���ϻ�����Ч���Ƽ��� CGA��HDF-��ϸ���ϵĹⱣ��ʾ��ͼ��CGAͨ��TGF-��-Smad2/3�źŴ����ٽ���ԭ����1�ĺϳɣ���ͨ���µ�MMP-1��MMP-3���ƽ�ԭ�����⡣���⣬CGA������UVA�յ���ROS�Ļ��ۣ�������DNA���˲��ٽ�ϸ�������Ӷ�������ϸ����������ɫ����T����DZ������;ֱ��ͷ������;����ͷ��DZ�ڼ��ECM��ϸ�������;MMP�����ʽ�������ø;���������������� ת���� 4. ���Ϻͷ��� 4.1. ϸ������ ����̥Ƥ������άϸ��CCC-ESF-1ϸ�����й�ҽѧ��ѧԺ����ҽѧ�о���ϸ����Դ���ģ��й�����Э��ҽѧԺ���ṩ��ԭ������Ƥ����άϸ��-���ˣ�HDF-����ϸ������ScienCell�о�ͼ��ݣ�����������������ʥ���Ǹ磩��CCC-ESF-1ϸ����Dulbecco�ĸ���Eagle��������DMEM��Gibco��������®�� �����Ƽ��������������ݿ���˹�͵£��������������� 10% ̥ţѪ�� ��FBS����Gibco����Ĭ�������Ƽ������������������ֶ�ɪķ���� 100 ��λ/mL ��ù�غ� 100 ��λ/mL ��ù�ء���HDF-��ϸ���ڳ���άϸ����������FM��ScienCell Research Laboratories��Inc.��������������ʥ���Ǹ磬������Cat. #2301������2%FBS������άϸ�������������FGS��ScienCell Research Laboratories��Inc.��ʥ���Ǹ磬�����������ݣ�������è#2352������ù��/��ù����Һһ�����������Щϸ����5%CO�ij�ʪ�����з���2 ��37��C�� 4.2. UVA ���� HDF-��ϸ����2.5��10���ܶȽ���5/6��������Ŀס�24Сʱ����PBS�滻����������¶��UVA��12J / cm2�� 60 ���ӡ�ʵ����ʹ�õ�UVAԴ���������������PURI Materials���й����ڣ������ֵ���䲨��Ϊ365 nm��UVA��¶����PBSϴ��ϸ����Ȼ����DMSO��0.1%�����գ���CGA��3��30��M������24Сʱ�Խ�һ��ʵ�顣 4.3. ����ͻ�ѧƷ �� abcam �����Խ�ԭ 1 ���������Ŀ��塣MMP3�� �ѽ����գ� Rad51�� ��-H2AX�� p-ERK1/2̩��202/̩��204��ERK��p-smad2/3��smad2/3����-����������Ӧ��HRP�ؽڶ�������Cell Signaling Technologies���������������ݵ���˹����MTT��DCFH-DA����Solarbio���й��Ϻ��������������¾�8466��CGA���ɰ��������¾�8466���й��ɶ����ṩ�������ʵ���Ũ���ܽ���DMSO�С� 4.4. ϸ�������ⶨ MTT��3-��4��5-��������-2-����-2��5-�����������廯��ⶨ�����ڲ���CGA����������Ƥ����άϸ���Ķ������á���HDF-��ϸ�����ֵ�96�װ��С���ҹ��ϸ����37��C���ò�ͬŨ�ȵ�CGA����24��48��72Сʱ�� Ȼ��MTT����Ũ�ȣ�0.5mg / mL����Һ����4Сʱ�����ȥ�������������H�����ܽ���DMSO�С�ø���ǣ�Biotek Instruments�� Inc.�� Winooski�� VT�� USA�����ڲⶨ570nm��������ȡ� 4.5. ���� RT-PCR ��qRT-PCR�� �ⶨ HDF-��ϸ������RNAͨ��Easypure RNA�Լ��У�Tansgen Biotech���й���������ȡ��cDNA �ǰ��������̵�˵��ʹ�� TransScript һ���� gDNA ȥ���� cDNA �ϳ� SuperMix �Լ��У��й�����̹˹������õġ�ʹ��SYBR��ɫPCRԤ��Һ�Լ��У�Cat.QPK-201���ձ�����ģ���ABI PRISM 7900���м��ϵͳ��Ӧ������ϵͳ�����������������ݸ�˹�سǣ�������qPCR���������£� ��2.GAPDH�������ڲ����ơ�ָʾ�Ļ��������� 2−����Ct ������ ��2 qRT-PCRʵ���е��������С�
4.6. ������ӡ���ⶨ CGA������HDF-��ϸ���ñ����RIPA�ѽ��Һ�ѽ�30���ӡ�ͨ��SDS-PAGE����������Һ�ĵ��������ʽ��У���������ת�Ƶ�PVDFĤ�ϣ�������������٣����������ݣ�����������5%BSA��պ���������һ��̽��Ĥ��������Ӧ��HRPż��������һ��������Ȼ����Tanon Chemishinecence Substrates���ӻ������ʣ���Image Quant LAS 4000��GE Healthcare��Ƥ˹����Τ���������ݣ���������¼������Image JApp���з����� 4.7. �����Խ�ԭ����� ��HDF-��ϸ����1��10���ܶȽ�����24�װ���5 ϸ��/�����û�ϲ�ͬŨ�ȵ�CGA����ϸ����48Сʱ���ռ�����Һ����ʹ��SirCol��ԭ���ײⶨ����Biocolor��������˹�أ��������������ܿ����Խ�ԭ���ס�������Щʵ�飬���Ӵ�������ϸ������ȡ�� 100 ��L ����Һ�� 1 mL �����Ǻ�Ⱦ�ϣ�һ��������Ⱦ�ϣ��ڲⶨ����������Բ�����ԭ�����ŷ��������Է�Ӧ��Ȼ����������������ת���� 30 ���ӡ��� 12��000 rpm ���� 10 ���Ӻ��� 750 ��L ���������ϴ���Լ��Գ�ȥδ��ϵ�Ⱦ�ϡ������250��L���Լ������ܽ⽺ԭ����ϵ�Ⱦ�ϣ������������̵�˵����555nm����������ȣ�Biotek������ҵ���������� ʹ�òⶨ���ṩ��I�ͽ�ԭ����У��Ʒ��ñ����ߡ� 4.8. �����ͼ�������� ���о�ʹ���˰˸�BioMAPϵͳ���Կ��ٱ���CGA���ܡ���BioMAP HDF3CGFϵͳ�У�ԭ��������������Ƥ����άϸ����HDF-n���ڵ�Ѫ�������½���24Сʱ��Ȼ����ϸ�����Ӵ̼� ��1 ��ָ��������CGA����72Сʱ��һ�������־������ʣ������� ��1 ��ELISA���������о���ʹ�õķ�����ǰ�������ķ���������ͬ[31]. 4.9. ϸ�������ⶨ HDF-��ϸ����UVA���䣨12 J / cm������CGA����2).����24Сʱ���ջ�HDF-��ϸ����������100��LȾɫ����Һ�С�Ȼ���� 5 ��L Ĥ������ V-APC �� 10 ��L �⻯��� ��PI�� ���ںڰ��з��� 5 ���ӡ�ʹ����ʽϸ������BD FACSVerse���������ں�����ϸ������ϸ���ͻ���ϸ����BD�����ѧ������������������ʥ�������� 4.10.ϸ�� ROS ���ⶨ ��HDF-��ϸ����3��10���ܶȽ�����6�װ���5 ϸ��/������UVA���䣨12J / cm���������û�û��CGA����Ũ��Ϊ3��30��M������ϸ��2).����24Сʱ���ռ�HDF-��ϸ���������������̵�˵��ʹ��DCFH-DA ROS̽��ʹ�û������ⶨ�Լ��У�Solarbio��CA1410���й��Ϻ����ⶨϸ����ROS�IJ�������HDF-��ϸ����37��C����5%COȾɫ10��M DCFH-DA��������ҺȾɫ30���ӡ�2.Ȼ���ջ�ϸ����ʹ��BD FACSVerse���з�����ʽϸ������ 4.11. ͳ�Ʒ��� ���ݱ�ʾΪʹ��һʽ����ֵ������ ��S.D�� �ľ�ֵ���Ƚ�ʹ��˫βѧ���� t-���ԡ����챻��Ϊ�� p ��0.05�� ת���� ȷ�� �༭��л��ҽ�ƴ�ѧ������̳ҽԺ�����������ı���Ĵ����������¾�8466�Ƽ���չ������ҵ�˾����Žܵ�֧�š� ת���� ��д
ת���� ������� �������ݿ�����ȡ https://www.mdpi.com/article/10.3390/ijms23136941/s1. �����˴���ȡ���������ļ�����231K��ѹ����ת���� �������� ���о����й�������Ȼ��ѧ����81703566�������� ת���� �༭���� ����ͷ����ۣ�N.X.��Y.L.;��ʽ���������ݹ�����J.J.��M.J.;д������ԭʼ�ݸ�������������;�ල����Ŀ������X.C.���б༭�����Ķ���ͬ���ѷ������ָ�汾�� ת���� �������ίԱ������ ���m�á� ת���� ֪��ͬ������ ���m�á� ת���� ���ݿ��������� ���ݰ����������С� ת���� �����ͻ �༭���������������ͻ�� ת���� ��ע ������ע�� MDPI���ѷ�����ͼ�ͻ���������ϵ�еĹ�ϽȨ���ű��������� ת���� ���� 1. ��˹ M.R.�� ������ T.�� ����˹ J.L.�� ����� L.F.�� ������˹ D.E.�� ����˹ M.�� ���� L.D.�� ��˹ R.J.S.�� ɳ����˹���� P.ʲô��˥�ϣ� ǰ�档���ڡ� 2012;3��134. DOI�� 10.3389/fgene.2012.00134. [PMC �������] [����ҽѧ] [��������] [GOOGLEѧ������]2. Brenneisen P.��Sies H.��Scharffetter-Kochanek K.������-B���պͻ��ʽ�������ø - ��ͨ���ź��յ�����ʼ�¼��� ��. N. Y. �����¿�ѧ. 2002;973:31�C43.DOI��10.1111/j.1749-6632.2002.tb04602.x�� [����ҽѧ] [��������] [GOOGLEѧ������]3. Hirobe T.��Osawa M.��Nishikawa S.I.�����ӿ�������������С���Ƥ��ɫ��ϸ������ֳ�ͷֻ��� ���ϡ�ϸ���ֱ��� 2003;16:644�C655.DOI��10.1046/j.1600-0749.2003.00092.x�� [����ҽѧ] [��������] [GOOGLEѧ������]4. Smith L.T.��Holbrook K.A.��Madri J.A.������̥��̥��Ƥ���е�I��III��V�ͽ�ԭ���ס� �����ء� 1986;175:507�C521.DOI��10.1002/aja.1001750409�� [����ҽѧ] [��������] [GOOGLEѧ������]5. Rittie L.��Fisher G.J.��Ȼ���������������Ƥ���ϻ��� ��Ȫ���������ӡ����к��� 2015;5��a015370.DOI��10.1101/cshperspect.a015370�� [PMC �������] [����ҽѧ] [��������] [GOOGLEѧ������]6. Verma R.P.��Hansch C.���ʽ�������ø��MMPs������ѧ����ѧ���ܺͣ�Q��SARs�� �����л�ҽѧ��ѧ 2007;15:2223�C2268.DOI�� 10.1016/j.bmc.2007.01.011. [����ҽѧ] [��������] [GOOGLEѧ������]7. ������ H.�� ����˹�� R.�� �Ἢ�� M.�� ���Ϳ� O.�� ������� F.�� ���� H.Ѫ����Ƥ�������ӣ���������ø������֯���Ƽ����л�ۺ�����Ѫ��Σ�����صĹ����� ŷ������ҽѧҩ��ѧ����ѧ. 2016;20:1015�C1022. [����ҽѧ] [GOOGLEѧ������]8. Kohl E.�� Steinbauer J.�� Landthaler M.�� Szeimies R.M. Ƥ���ϻ��� J. Eur. Acad. Dermatol.ά���ޡ� 2011;25:873�C884.DOI��10.1111/j.1468-3083.2010.03963.x. [����ҽѧ] [��������] [GOOGLEѧ������]9. Varani J.�� Dame M.K.�� Rittie L.�� Fligiel S.E.�� Kang S.�� Fisher G.J.�� Voorhees J.J. ��ʱ��˳���ϻ���Ƥ���н�ԭ�������ɼ��٣�����άϸ���������������Ըı�ͻ�е�̼�ȱ�ݵ����á� ���ж��� 2006;168:1861�C1868.DOI��10.2353/ajpath.2006.051302�� [PMC �������] [����ҽѧ] [��������] [GOOGLEѧ������]10. Quan T.�� Qin Z.�� Xia W.�� Shao Y.�� Voorhees J.J.�� Fisher G.J. ���ϻ��еĻ��ʽ����������ø�� J. ���顣Ƥ���С����졣 2009;14:20�C24.DOI�� 10.1038/jidsymp.2009.8. [PMC �������] [����ҽѧ] [��������] [GOOGLEѧ������]11. Zaid A.N.��Al Ramahi R.��Ȼ���ӵ�ɫ���ѰߺͿ�˥�����ơ� �����ҩ��ʦ 2019;25:2292�C2312.DOI��10.2174/1381612825666190703153730�� [����ҽѧ] [��������] [GOOGLEѧ������]12. Clifford M.N. ���������¾�8466������������� - ���ʣ���������ʳ������ J. ��ѧ. ʳƷũҵ 1999;79:362�C372.doi�� 10.1002/��SICI��1097-0010��19990301��79��3<362����AID-JSFA256>3.0.CO;2-D. [��������] [GOOGLEѧ������]13. ����ϼ�� �½����� �������� ����ΰ�� ������ ��־���� ����. ���������¾�8466��С��֬�����յ����Ըζ��Եı�������. ��ȼ��Res. 2010;59:871�C877.DOI��10.1007/s00011-010-0199-z�� [����ҽѧ] [��������] [GOOGLEѧ������]24�� ������ �ξ��� ������ �������� ���� ������. �۶�������������������������¾�8466������Կ��������������. ������ˡ�B. 2014;116:700�C706.DOI�� 10.1016/j.colsurfb.2013.11.010. [����ҽѧ] [��������] [GOOGLEѧ������]15. Ѧ���� ������ ������ ����� ������ �¾��� ������ �־��� ��� �ž��� ��.���������¾�8466ͨ��������ϸ���� M2 �������� M1 ���������ƽ���ĸϸ������������ ��ѧ���� 2017;7��39011. DOI�� 10.1038/srep39011. [PMC �������] [����ҽѧ] [��������] [GOOGLEѧ������]16. ��Τ�� M.�� �ռ��� V.�� ����˹ M.�� ���� A.A.�� �� G.J.�� ��ķ������ M.�� �������� F.�� �Ͱ����� D.�� �� F.F.�� Ī������-������ F.�� �Ȱ��������¾�8466��CGA����ҩ��ѧ��鲢������һ���о��� ����ҽѧ��ҩ������ 2018;97:67�C74.DOI�� 10.1016/j.biopha.2017.10.064. [����ҽѧ] [��������] [GOOGLEѧ������]17. Li H.R.�� Habasi M.�� Xie L.Z.�� Aisa H.A. ���������¾�8466��B16��ɫ����ϸ����ɫ�����ɵ�Ӱ��. ���ӡ� 2014;19:12940�C12948.DOI��10.3390/����190912940�� [PMC �������] [����ҽѧ] [��������] [GOOGLEѧ������]18. �������� �����ܣ� ������� Ҧ־ΰ�� ֣���� �������� ��־�֣� �����飬 ��������Ӱ��������¾�8466�ɼ�����HaCaT�����γ�ϸ����UVB�鵼������Ӧ���� ����Ħ����ɪ�� 2014;22:136�C142.DOI�� 10.4062/biomolther.2014.006. [PMC �������] [����ҽѧ] [��������] [GOOGLEѧ������]19. ����Y.�� Lee T.K.�� Kim J.D.�� Kim B.�� Sim H.�� Lee J.C.�� Ahn J.H.�� Park J.H.�� Lee J.W.�� Hong J.�� et al. �������������¾�8466��«����Ұӣ�Һڹ���ȡ��ľֲ�Ӧ��ͨ������С��ԭ�����ƻ�������UVB�յ���Ƥ�����ˡ� ���ӡ� 2020;25��4577. DOI�� 10.3390/����25194577. [PMC �������] [����ҽѧ] [��������] [GOOGLEѧ������]20. Girsang E.��Ginting C.N.��Lister I.N.E.��Gunawan K.Y.��Widowati W.���������¾�8466���������յ��ij���άϸ���Ŀ��Ϳ�˥�����ԡ� ����� 2021;9��e11419.DOI��10.7717/peerj.11419�� [PMC �������] [����ҽѧ] [��������] [GOOGLEѧ������]11�� Chung J.H.�� Seo J.Y.�� Lee M.K.�� Eun H.C.�� Lee J.H.�� Kang S.�� Fisher G.J.�� Voorhees J.J. �˾���ϸ���������Ե���ø������Ƥ���е������ߵ��� �����ڡ� J. ���顣Ƥ���С� 2002;119:507�C512.DOI��10.1046/j.1523-1747.2002.01844.x�� [����ҽѧ] [��������] [GOOGLEѧ������]22. ������ D.�� ������ŵά�� M.G.�� ά����� S.�� ����ƽ�� �� N.�� ������ A.�� �¶�˹ T.�� ����� D.�� ������ M.�� �� C.B.�ӻƴ������Ϳ�˥�ϻ��ƣ��յ���Ƥ���Ե��ϳɺ͵��Ե�����ά�γɡ� ���� J. ��˹÷�ء���ѧ. 2011;33:62�C69.DOI�� 10.1111/j.1468-2494.2010.00588.x. [����ҽѧ] [��������] [GOOGLEѧ������]23. Purohit T.��He T.��Qin Z.��Li T.��Fisher G.J.��Yan Y.��Voorhees J.J.��Quan T.����Ƥ����άϸ����I�ͽ�ԭ����Smad3�����Ե��ڣ�������Ƥ�������֯˥�ϵ�Ӱ�졣 J.�����ж�����ѧ. 2016;83:80�C83.DOI�� 10.1016/j.jdermsci.2016.04.004. [����ҽѧ] [��������] [GOOGLEѧ������]14�� Bhogal R.K.��Bona C.A.ϸ�����źŵ��ڼ�ø��ERK����IL-4��IL-13�̼�������Ƥ����άϸ����I�ͽ�ԭ�ϳɵĵ������á� ������������ѧ�� 2008;27:472�C496.DOI��10.1080/08830180802430974�� [����ҽѧ] [��������] [GOOGLEѧ������]25. Gonzaga E.R. �������ڹ����ˡ�Ƥ���ϻ���Ƥ�����е����ã��Ᵽ������Ҫ�ԡ� ���֡�Ƥ���С� 2009;10������1����19�C24.DOI��10.2165/0128071-200910001-00004�� [����ҽѧ] [��������] [GOOGLEѧ������]26. Landau M. Ƥ���ϻ�����Դ�����ء� �������š�Ƥ���С� 2007;35:1�C13. [����ҽѧ] [GOOGLEѧ������]27. Inagaki Y.��Truter S.��Ramirez F.ת����������-��ͨ������Sp1���λ���˳ʽ����Ԫ���̼��� 2��I����ԭ�������� J. ���ﻯѧ 1994;269:14828�C14834.DOI��10.1016/S0021-9258��17��36699-1�� [����ҽѧ] [��������] [GOOGLEѧ������]28. Choi S.I.�� Jung T.D.�� Cho B.Y.�� Choi S.H.�� Sim W.S.�� Han X.�� Lee S.J.�� Kim Y.C.�� Lee O.H. ����ũ����Ʒ�������ߵĿ����ϻ����� Birradi ��ëС��Ƥ��. ���� J. Ħ��ҽѧ 2019;44:559�C568. [PMC �������] [����ҽѧ] [GOOGLEѧ������]29. �� X.�� �� R.�� ʩ H.�� �� X.�� �� Y.�� ���� A.�� �� C. �����ض������� A �����յ�������Ƥ����άϸ�����ϻ��ı�������. Ħ��ҽѧ���� 2018;17:7227�C7237. [PMC �������] [����ҽѧ] [GOOGLEѧ������]30. Hwang B.M.�� Noh E.M.�� Kim J.S.�� Kim J.M.�� You Y.O.�� Hwang J.K.�� Kwon K.B.�� Lee Y.R. ������ͨ����������Ƥ����άϸ���е� MAPK-p38/JNK ;�������� UVB �յ��Ļ��ʽ�������ø-1/3 ��� Exp. Dermatol. 2013;22:371�C374.DOI��10.1111/exd.12137�� [����ҽѧ] [��������] [GOOGLEѧ������]31. Berg E.L.��Yang J.��Melrose J.��Nguyen D.��Privat S.��Rosler E.��Kunkel E.J.��Ekins S.��ԭ������ϸ��ϵͳ�ж���Ļ�ѧ�б��;�����Ի��ơ� ҩ��ѧ��־������ѧ�������� 2010;61:3�C15.DOI�� 10.1016/j.vascn.2009.10.001. [����ҽѧ] [��������] [GOOGLEѧ������]
�������� ���ʷ��ӿ�ѧ��־ �˴��ṩ ��ѧ�����ֳ���ѧԺ ��MDPI�� | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
��һƪ�����������¾�8466ͨ��ACAT1-TPK1-PDH;���յ���ĸϸ����ϸ���ֻ�
��һƪ������ҵ�μӵ������й���Ͷ��Ტ���������ٴ������� |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

 ͼ1
ͼ1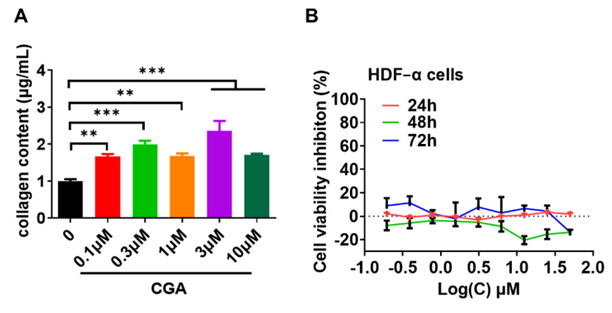 ͼ2
ͼ2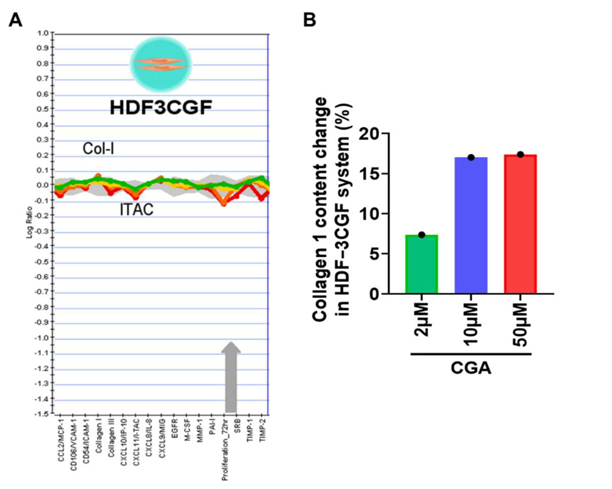 ͼ3
ͼ3
 ͼ4
ͼ4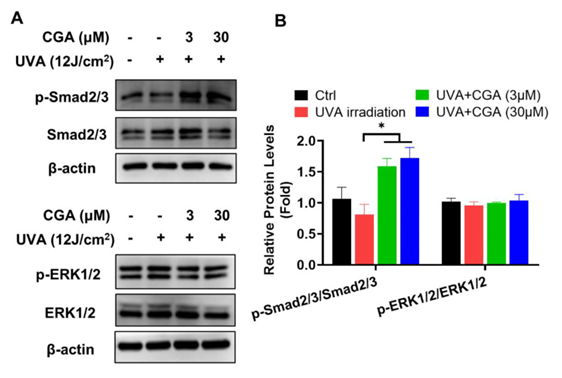 ͼ5
ͼ5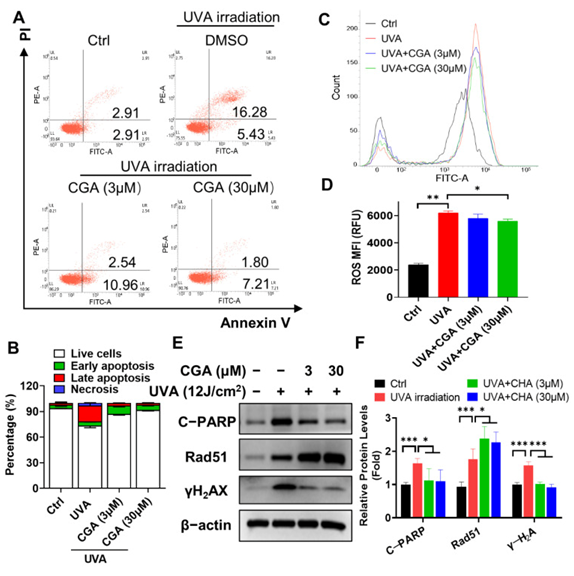 ͼ6
ͼ6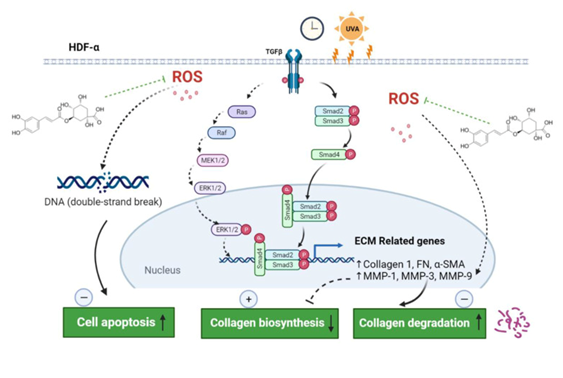 ͼ7
ͼ7