加入收藏 | 设为澳门新浦新京8466 | 中文 | English
 咨询热线: 028-85121781
咨询热线: 028-85121781

| Nat Commun:一种克服免疫检查点组织疗法耐受性的黑色素瘤潜在靶点 | ||||||||||||||||||||||
| [ 来源:转载自网络 发布日期:2022-10-14 09:58:51 责任编辑: 浏览次 ] | ||||||||||||||||||||||
|
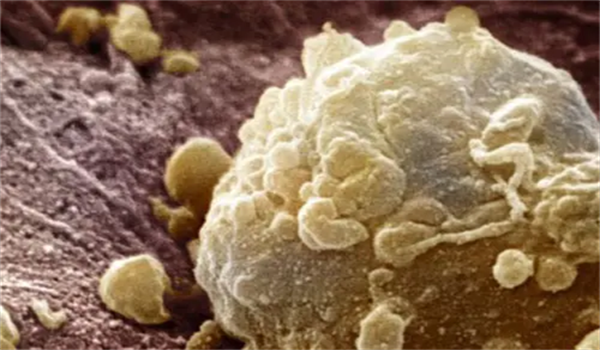
免疫检查点阻滞疗法(ICBs)已经彻底改变了多种晚期癌症的治疗方法,其中就包括黑色素瘤,然而四分之三的晚期黑色素瘤患者都会对免疫检查点阻滞疗法产生耐受性。肿瘤失去干扰素γ信号是抵御两种ICB药物(抗CTLA-4和抗PD-1)产生耐受性的主要机制,然而,克服这种耐受性的方法让研究人员仍然难以捉摸。 近日,一篇发表在国际杂志Nature Communications上题为“Selective suppression of melanoma lacking IFN-γ pathway by JAK inhibition depends on T cells and host TNF signaling”的研究报告中,来自阿拉巴马大学等机构的科学家们通过研究揭示了一种潜在的靶点,或能利用临床批准的药物鲁索替尼(ruxolitinib)来抑制对ICB耐受的黑色素瘤。
人类黑色素瘤中干扰素γ信号的缺失或许是由干扰素γ信号通路中基因的功能失调所引起的,然而,在小鼠模型中,敲除突变或许并不能揭示肿瘤细胞中的干扰素γ信号的缺失如何调节肿瘤浸润性T细胞(TILs)的活性,因为这些模型仍然会含有一些干扰素γ信号;肿瘤浸润的免疫细胞对于癌症的控制非常重要,因为其能帮助检测并破坏肿瘤;然而,作为一种反击,癌症就会学习如何通过提高细胞表面的免疫检查点蛋白来躲避这种破坏,而这些表面蛋白则能向肿瘤浸润的T细胞发送“关闭”信号。 因此,研究人员通过敲除干扰素γ信号的受体基因开发了一种更为洁净的小鼠黑色素瘤模型,他们利用这种改进型的模型(IFNγR1KO)来探究癌细胞对ICB疗法的耐受性机制,以及IFNγR1KO黑色素瘤如何改变肿瘤浸润T细胞对ICBs的反应。与非敲除的黑色素瘤相比,小鼠IFNγR1KO黑色素瘤或能表现出肿瘤浸润T细胞水平的降低,比如CD8 杀伤性T细胞等;而且肿瘤浸润T细胞还能降低抵御肿瘤的免疫反应,这或许就表明,黑色素瘤中正常的干扰素γ信号或许在塑造肿瘤浸润T细胞上扮演着重要角色,通过证实这些临床发现,研究人员对来自癌症基因组图谱中人类黑色素瘤的数据进行生物信息学分析,结果发现,携带干扰素γ信号减弱的黑色素瘤或许会降低T细胞特征基因的表达,这就表明T细胞浸润和功能水平的降低。 从机制上来讲,IFNγR1KO小鼠黑色素瘤中或许存在一种持续性激活的蛋白酪氨酸激酶王阔,其以激活的JAK1/2激酶为中心,这种细胞内的信号通路或许能通过激活的mTOR信号所介导。鲁索替尼是一种JAK1/2的抑制剂,研究者发现,该药物能抑制IFNγR1KO黑色素瘤的癌症生长,但并不会影响对照模型黑色素瘤的生长;实验性地剔除T细胞或宿主肿瘤坏死因子信号或能完全废除鲁索替尼的效应,这或许就让研究人员得出结论,鲁索替尼对IFNγR1KO黑色素瘤的抑制效应依赖于T细胞和宿主细胞因子肿瘤坏死因子;此外研究者还发现,鲁索替尼能通过重编程肿瘤浸润的T细胞(而不是直接通过杀灭肿瘤细胞)来介导其治疗性效应。 目前他们正在通过深入研究揭示对JAK1/2的抑制是否能作为一种绕过黑色素瘤患者对ICB疗法耐受的新型策略,这目前是一个非常迫切的未满足的医疗需求。 综上,本文研究结果揭示了肿瘤内在的干扰素γ信号在塑造肿瘤浸润T细胞上的重要角色,同时也揭示了一种能绕过干扰素γ信号缺陷的黑色素瘤抵御ICB疗法的一种新型靶向性疗法。 慎重声明:本文版权归原编辑所有,转载文章仅为传播更多信息之目的,如编辑信息标记有误,请第一时间联系大家修改或删除。 | ||||||||||||||||||||||
|
上一篇:BBRC:揭示如何降低黑色素瘤疗法的耐受性
下一篇:Mol Cell:增强抑制蛋白p53信号和机体肿瘤抑制的新型分子机制 |
||||||||||||||||||||||
| ||||||||||||||||||||||