加入收藏 | 设为澳门新浦新京8466 | 中文 | English
 咨询热线: 028-85121781
咨询热线: 028-85121781

| Science:工程化T细胞受体减少脱靶毒性 | ||||||||||||||||||||||
| [ 来源:转载自网络 发布日期:2022-04-18 09:50:48 责任编辑: 浏览次 ] | ||||||||||||||||||||||
|
T细胞受体(TCR)控制T细胞抗原特异性,并在识别肽-主要组织相容性复合体(peptide–major histocompatibility complex, pMHC)时帮助确定反应敏感性。在免疫疗法中,与肿瘤抗原发生反应的TCR用于过继性细胞疗法(ACT)中根除肿瘤,但大多数内源性肿瘤特异性TCR引起的功能反应很弱。为了克服这一限制,肿瘤反应性TCR经历亲和力成熟,以提高其杀伤力。然而,高亲和力的TCR在临床试验中可表现出脱靶毒性,这表明需要新的治疗方法。工程化TCR显示对肿瘤靶标的高效力,同时保留较低的生理亲和力,有可能提高T细胞疗法的疗效,而不增加脱靶副作用的风险。抓键(catch bond)在不断增加的作用力下延长了蛋白之间的结合寿命,从而在pMHC接触时触发TCR激活。然而,抓键是否可以被设计来提高TCR的效力,以及这类TCR是否会保留其天然的特异性和亲和力,目前还不清楚。 在一项新的研究中,来自斯坦福大学和犹他大学等研究机构的研究人员提出需要一种替代亲和力成熟的策略来赋予临床上有用的高效力但低亲和力的TCR[即三维结合亲和力(KD)为~5至50μM]。因此,他们设计了一种称为“抓键搜寻(catch bond fishing)”的工程化策略,它依赖于一种功能选择来招募反应性差的TCR和pMHC之间的抓键。他们推测,通过将某些TCR残基突变成由带电荷或极性氨基酸组成的小文库,然后筛选高效力、低亲和力的TCR变体,可以获得新的抓键。相关研究结果发表在2022年4月8日的Science期刊上,论文标题为“Tuning T cell receptor sensitivity through catch bond engineering”。
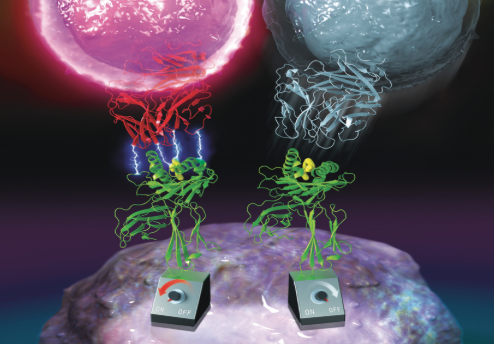
研究者们将工程化策略应用于HIV肽特异性人类TCR(TCR55),TCR55以生理上的三维结合亲和力结合人类淋巴细胞抗原B35(HLA-B35)-HIV复合物,但由于在细胞上明显缺乏抓键的形成,正如生物膜力探针(biomembrane force probe, BFP)所测量的那样,未能激活下游的信号传导。他们的功能选择分离出了CD69高表达和pMHC四聚体染色低的T细胞,从而富集了在低亲和力下触发的抓键工程化TCR(即获得抓键的工程化TCR)。TCR55的α和β链上的单个氨基酸位置是抓键热点,在这些位置上的几个氨基酸替换导致强大的信号传导,尽管保留了生理上的三维结合亲和力。根据细胞上的BFP检测,这些具有信号传导活性的TCR变体获得了抓键,它们较长的结合寿命与信号强度相关。 随后,将这种抓键工程化策略应用于黑色素瘤抗原MAGE-A3特异性TCR,这种TCR的亲和力成熟版本TCR-A3A,以前曾被用于临床试验,由于HLA-A2呈现来自心血管组织衍生的TITIN分子的肽而引起的脱靶毒性,导致患者死亡。他们分离出几个高效力、低亲和力的亲本TCR变体,它们能以生理亲和力(KD为大约10~50μM)促进杀伤MAGE-A3阳性的癌细胞系。此外,这些抓键工程化TCR变体与表达TITIN肽的细胞没有明显的交叉反应。他们使用一个酵母展示的HLA-A1肽文库来筛选抓键工程化TCR变体的交叉反应性。他们发现,预测的人类自我抗原的交叉反应性与它们的亲和力成熟的TCR-A3A对应物相比,可忽略不计。 综上所述,这些编辑发现TCR和pMHC之间的抓键获得是一种可工程化的参数,可以直接提高TCR的敏感性,而对三维结合亲和力影响不大。此外,TCR的敏感性可以通过不同水平的峰值结合寿命进行精确的微调。对临床上有用的、肿瘤反应性的TCR进行抓键工程化是一个替代亲和力成熟的可行方案,可以产生高效力、低亲和力的TCR,从而减少免疫治疗中脱靶毒性的可能性。 慎重声明:本文版权归原编辑所有,转载文章仅为传播更多信息之目的,如编辑信息标记有误,请第一时间联系大家修改或删除。 | ||||||||||||||||||||||
|
上一篇:Radiology:胶质瘤大脑血管功能失调研究取得的进展
下一篇:PNAS:揭示卵巢癌抵抗免疫疗法机制 |
||||||||||||||||||||||
| ||||||||||||||||||||||